ביוכימיה - פרק 1 : כימיה כללית
- 191 שאלות
- 72 תגובות
- 0% הושלמו
- equalizer סטטיסטיקות
- share שתף
Discuss, Learn and be Happy דיון בשאלות
help
brightness_4
brightness_7
format_textdirection_r_to_l
format_textdirection_l_to_r
כדי שתגובה תהיה ספונטנית (סמן את הלא נכון)
1
| done | ||
מיין לפי
מוניטין: 1
אם נשליך את המשוואה לחישוב אנרגייה חופשית על תא חי
נראה שהוא למשל צורך אנרכיה מהשמש אבל פולט את אותה כמות של אנרגיה בצורת חום לסביבה ומוביל לעלייה באנטרופיה של הסביבה
מה מהבאים אינו נכון לגבי תא חי?
1
| done |
מה אינו נכון לגבי הדלתא G בתנאים הסטנדרטיים
1
| done |
מיין לפי
מוניטין: 1
שתי קונבנציות (הנחות שמקובלות ורווחות בקרב הרוב) שצריך להכיר -
1. כשיש תגובה שמגנזיום הוא יון שדרוש ע"מ לתווכה (לרוב תגובות שמערבות ATP) נהוג להניח שריכוז יון המגנזיום הוא 1 מילי מולאר.
2. בתגובות שמערבות מים, יוני מימן או מגנזיום, הריכוזים שלהם לא ייכתבו כחלק מהמשוואה אלא יוגדרו כחלק מהקבועים דלתא G בתנאים סטנדרטיים וטאג או קבוע שיווי המשקל וטאג (שהוא קבוע בתנאים ביוכימיים סטנדרטיים חומציות וריכוז המים מהשאלה הם התוספות )
מה ניתן להסיק מהמשוואה הבאה
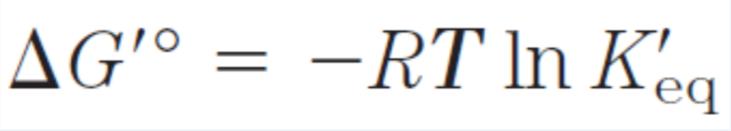
1
| done |
מה לא ניתן לקבוע בהתאם לשני הגרפים הבאים:
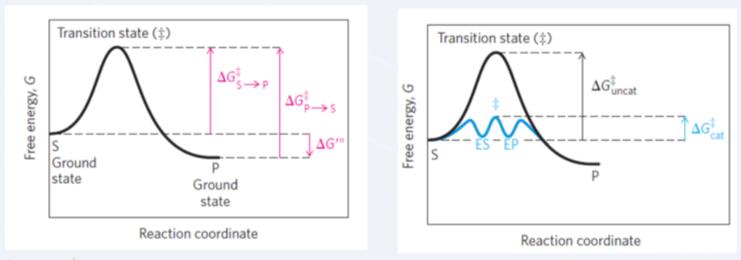
1
| done | ||
מיין לפי
מוניטין: 1
הקרטריון לספונטניות הוא דלתא G שלילי ולא התנאים הסטנדרטיים.
אם נשמור על ריכוז נמוך של התוצרים מנת התגובה תהיה קטנה מ- 1 ותתקבל תוצאה שלילית ב- ln וכך התגובה תתקדם קדימה.
חלק מהאנרגיה תמיד אובד לצורך הגדלת האנטרופיה וכמות האנרגיה שמופקת מהתגובה תמיד תהיה קטנה מהערכים התאורטיים.
מוניטין: 1
עץ יהיה יציב יותר (מועדף יותר מבחינה תרמודינמית) כאשר יפורק לפדח ולמים אך למה הם אינם ניצתים באופן טבעי?
כנראה בגלל אנרגיית האקטיבציה חיובית מאוד. ברגע שתסופק אנרגיית האקטיבציה למשל בצורת גפרור, האנרגיה שתתקבל מבעירת נקודה מסוימת בעץ תספיק לשפעול תהליך זה בסביבה קרובה לנקודה ו וכך התהליך ימשיך עד בעירה מוחלטת או עד לעצירת התהליך.
מוניטין: 1
בגרף מימין, כיוון שחימום המערכת לטמפ' גבוהות לא בא בחשבון בתאים חיים האנזימים מייצבים מצבי ביניים שונים וכך מקטינים את אנרגיית האקטיבציה.
חשוב להבין שהשינוי באנרגיה החופשית של המערכת לאחר תגובה הוא זהה בין אם התגובה התרחשה באופן ספונטני עם אנרגיית אקטיבציה גבוהה או שזורזה על ידי אנזים.
השינוי באנרגיה החופשית תלוי רק בריכוזי המגיבים והתוצרים בשוו"מ ובטמ"פ של המערכת
נתונות התגובות הבאות: 1- גלוקוז+ פוספט ----> גלוקוז -6- פוספט+ מים דלתא ג'י= 13.8 (קילוג'אול למול) 2- אי-טי-פי+ מים ----> אי-די-פי + פוספט חופשי דלתא ג'י= 30.5- (קילוג'אול למול) קבוע שיווי משקל 1 הוא 0.0039 קבוע שוו"מ 2 הוא 200,000 וקבוע שוו"מ של התגובה המצומדת הוא 7800 (הדלתא ג'י הוא בתנאים סטנדרטיים ביוכימיים) מה לא נכון ?
1
| done | ||
| done |
מיין לפי
הקינטיקה מתארת את ה_____ ואילו התרמודינמיקה מתארת_________
1
| done |
לא ניתן לקבוע בכל מערכת ספונטנית בטבע האם הכוח שלוקח אותה קדימה הוא האנתלפיה, האנטרופיה או שניהם. העיקר שגיבס שלילי.
1
| done | ||
מיין לפי
בהמסת מי מלח - גם ה- H וגם ה- S חיוביים כלומר הכוח התרמודינמי שלוקח את הריאקציה קדימה הוא השינוי באנטרופיה. במקרה זה השינוי באנתלפיה דווקא מתנגד לספונטניות
1
| done | ||
מיין לפי






